Autor/a: Dres. Jin LX, Pitt SC, Hall BL, Pitt HA Surgery 2013; 154(2): 266-73
Introducción
El carcinoma de vesícula es la neoplasia maligna biliar más común y el 7º cáncer gastrointestinal más común [1]. Esta enfermedad maligna es altamente letal, con una tasa de sobrevida a 5 años < 5%, para aquellos pacientes con enfermedad no tratable mediante resección quirúrgica [2,3]. Una resección R0 completa es el estándar de cuidado en los pacientes con enfermedad localizada y la única terapia definitiva potencialmente curable [4-6]. Dado que la mayoría de los casos de cáncer de vesícula es diagnosticada en estadio avanzado, las resecciones mayores, incluyendo la hemihepatectomía, trisegmentectomía y duodenopancreatectomía, pueden ser requeridas para lograr márgenes negativos. En años recientes, el concepto de que esos pacientes se benefician de un manejo operatorio agresivo con resección radical, ha sido cada vez más aceptado [7].
La sobrevida a largo plazo para los pacientes con cáncer de vesícula ha sido bien documentada y es altamente dependiente del estadio al momento de la presentación [7-10]. Sin embargo, los datos sobre los resultados a corto plazo en grandes cohortes de pacientes sometidos a tratamiento quirúrgico son menos comunes. Los reportes de instituciones aisladas han mostrado que la mortalidad operatoria para el cáncer de vesícula ha ido disminuyendo a medida que las técnicas quirúrgicas y el manejo perioperatorio han mejorado [5-8,11,12]. Las tasas de mortalidad de las resecciones mayores para el cáncer avanzado de vesícula, sin embargo, permanecen altas en relación con muchas otras operaciones gastrointestinales [13,14]. Por lo tanto, los objetivos de este estudio fueron caracterizar los procedimientos quirúrgicos realizados en pacientes con cáncer de vesícula y los resultados perioperatorios asociados, en una cohorte multicéntrica grande en Norteamérica.
Métodos
El American College of Surgeons-National Surgical Quality Improvement Program (ACS-NSQIP)
El ACS-NSQIP es un registro multicéntrico basado en resultados ajustados por riesgo, con el objetivo de mejorar la calidad de la atención quirúrgica [15]. Ciento treinta y seis variables preoperatorias (características de los pacientes), intraoperatorias (procesos de atención) y postoperatorias (resultados adversos) son recolectadas por revisores clínico-quirúrgicos entrenados y certificados. Los resultados son evaluados a los 90 días después de la operación y se usan definiciones altamente estandarizadas y validadas.
Durante el período de estudio, el ACS-NSQIP usó un proceso sistemático de muestreo al azar, que abarcó un ciclo de 8 días, mientras que los primeros 40 casos que llenaron los criterios de inclusión y exclusión fueron evaluados. Los pacientes menores de 18 años fueron excluidos. Los datos sobre calidad fueron monitoreados mediante auditorías de confiabilidad inter calificadores así como soporte en línea para decisiones. Los datos fueron obtenidos de los ACS-NSQIP Participants Use Files, desde el 1 de enero de 2005 hasta el 31 de diciembre de 2009. Ese período de tiempo representa los primeros 5 años de datos del ACS-NSQIP. Durante ese tiempo, participaron 243 centros; 54% fueron académicos.
Procedimientos quirúrgicos
Los códigos primario y secundario para procedimientos de la Common Procedural Terminology, tal como fueron registrados en el ACS-NSQIP, se usaron para agrupar a los pacientes en uno de los siguientes 6 grupos de procedimientos: (1) diagnóstico; (2) colecistectomía; (3) hepatectomía parcial; (4) hepatectomía extendida; (5) paliación y (6) otro. Los procedimientos diagnósticos incluyeron sólo laparoscopía o laparotomía, con o sin biopsia. La colecistectomía incluyó procedimientos laparoscópicos y abiertos sin hepatectomía concomitante o cualquier otro procedimiento paliativo. La hepatectomía parcial incluyó resecciones en cuña, pero excluyó las hepatectomías derecha e izquierda. La hepatectomía extendida incluyó a las hepatectomías derecha, izquierda y extendida (más de 3 segmentos). Para los pacientes sometidos a hepatectomía, el número de anastomosis bilioentéricas concomitantes también fue registrado. Los procedimientos paliativos incluyeron procedimientos de derivación biliar, gastroyeyunostomía y esplanicectomía con alcohol, sin remoción de la vesícula y/o el hígado. Todos los otros procedimientos que no estuvieron relacionados directamente con el cáncer de vesícula subyacente fueron excluidos del análisis ulterior.
Pacientes con cáncer de vesícula
Los pacientes mayores a 18 años de edad que fueron sometidos a un procedimiento quirúrgico por cáncer de vesícula, fueron identificados mediante los códigos 156 o 156.0 asignados postoperatoriamente en la International Classification of Diseases, 9º edición (ICD-9). Los pacientes con diagnóstico de: (a) malignidad del hígado y de la vía biliar intrahepática (código 155 de la ICD-9), (b) malignidad de la vía biliar intrahepática (código 155.1 de la ICD-9), (c) malignidad de la vía biliar extrahepática (código 156.1 de la ICD-9), (d) malignidad de otros sitios especificados de la vesícula y de la vía biliar extrahepática (código 156.8 de la ICD-9) o (e) malignidad del tracto biliar en sitio no especificado (código 167.9 de la ICD-9), fueron excluidos.
Se recogieron 25 factores demográficos por cada paciente. El ACS-NQIP define al “cáncer diseminado” como (a) diseminación a uno o más sitios además del sitio primario y (b) cuando la presencia de metástasis múltiples indica que el cáncer está ampliamente diseminado, es fulminante o casi terminal. La ictericia fue definida como una medición de bilirrubina total > 1,5 mg/dL, antes del procedimiento. Los datos estuvieron disponibles en el 89,2% de los pacientes.
Resultados
Múltiples resultados fueron evaluados postoperatoriamente a los 30 días, en relación a si el paciente permanecía hospitalizado, había egresado o había sido readmitido en la misma o en otra institución. Todas las causas de mortalidad a los 30 días, así como la morbilidad global y la grave, fueron evaluadas. La morbilidad grave fue definida como la infección del sitio quirúrgico, órgano o espacio (ISQ), dehiscencia de la herida, evento neurológico, paro cardíaco, infarto de miocardio, embolia pulmonar, dependencia del respirador, insuficiencia renal progresiva o aguda y sepsis o shock séptico. Los eventos neurológicos incluyeron ictus o accidente cerebrovascular, coma por más de 24 horas o déficit neurológico periférico. La morbilidad global incluyó cualquier morbilidad grave, así como ISQ superficial o profunda, neumonía, reintubación no planificada, infección del tracto urinario (ITU) o trombosis venosa profunda (TVP). Toda ISQ fue definida como superficial, profunda, de órgano-espacio o dehiscencia de la herida. El retorno a la sala de operaciones y la duración de la estadía hospitalaria también fueron registrados.
Análisis estadísticos
Las características demográficas, mortalidad, morbilidad grave y morbilidad global, así como los otros resultados descritos, fueron comparados usando la prueba de 2 para las variables categóricas y el análisis de la varianza con la prueba t de Student para las variables continuas. La significación fue fijada en P < 0,05. El programa STATA, versión 11.0 (StataCorp LP, College Station, TX) fue usado para todos los análisis estadísticos.
Resultados
Procedimientos quirúrgicos
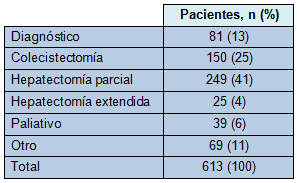
Un total de 613 pacientes con cáncer de vesícula fueron identificados (Tabla 1). Se realizó un procedimiento diagnóstico en el 13% y uno a más procedimientos paliativos en el 6%. Un procedimiento potencialmente curativo fue completado en 424 pacientes (69%). De esos pacientes, la distribución fue: colecistectomía 35%, hepatectomía parcial 59% y hepatectomía extendida en 6%. Entre los 249 pacientes que fueron sometidos a hepatectomía parcial, 13 (5,2%) tuvieron también una anastomosis bilioentérica. Entre los 25 pacientes con hepatectomía extendida, seis (24%) también tuvieron una anastomosis bilioentérica. Entre los “otros” pacientes, 12 fueron sometidos a duodenopancreatectomía, pero no se realizó una hepatectomía y pancreatectomía combinadas en ningún paciente.
• TABLA 1: Procedimientos quirúrgicos
Pacientes con cáncer de vesícula
La mediana de la edad de los pacientes fue de 67 años (rango intercuartilar [RIC]: 59-75) y el 65% fueron mujeres (Tabla 2). Los pacientes sometidos a colecistectomía tuvieron mayor edad (P < 0,001; mediana 73 años) comparado con los pacientes que fueron sometidos a hepatectomía extendida (63 años). Los pacientes que recibieron procedimientos paliativos tuvieron también más edad (mediana 70 años; RIC: 60-75). En todos los grupos de procedimientos hubo más mujeres que hombres; no obstante, en los pacientes que tuvieron procedimientos diagnósticos, la proporción de mujeres (51%) fue menor (P < 0,05). La mayoría de los pacientes eran blancos (65%), pero la distribución racial varió (P = 0,004) entre los grupos de procedimientos. La clase ASA (American Society of Anesthesiologists) también varió (P = 0,009), con un mayor porcentaje de pacientes con hepatectomía extendida siendo más sanos, con una clase ASA 2 (alteración menor).
• TABLA 2: Datos demográficos de los pacientes por procedimiento operatorio (Ver tabla)
Todos los 25 pacientes que fueron sometidos a hepatectomía extendida eran también funcionalmente independientes. Tanto los pacientes que tuvieron una hepatectomía parcial como los de hepatectomía extendida, tuvieron mayor probabilidad de ser independientes que los pacientes sólo con colecistectomía (97% y 100%, respectivamente, vs 91%; P < 0,02). El 14% de los pacientes colecistectomizados fue operado de manera ambulatoria, mientras que todos los de los otros grupos de procedimientos tuvieron más del 90% de los pacientes clasificados como internados (P < 0,001). Fue menos probable una operación de emergencia con la hepatectomía parcial (0,8%) y extendida (0%) y más probable (8%) con los procedimientos paliativos (P < 0,04).
La información sobre las comorbilidades de los pacientes se presenta en la Tabla 3. Los grupos quirúrgicos no difirieron con respecto a la obesidad, diabetes, uso de alcohol, tabaco o esteroides. Los grupos fueron también similares con respecto a la enfermedad pulmonar obstructiva crónica (EPOC), insuficiencia cardíaca congestiva, enfermedad coronaria o vascular periférica y desórdenes neurológicos. Los pacientes sometidos a hepatectomía extendida tuvieron mayor probabilidad (P < 0,001) de tener un cáncer diseminado al momento de la primera operación (16%), comparado con los pacientes sometidos a colecistectomía (3%) o hepatectomía parcial (5%). Similarmente, los pacientes que recibieron procedimientos paliativos tuvieron mayor probabilidad (P < 0,01) de tener un cáncer diseminado (18%) y pérdida substancial de peso (28%), así como de haber recibido recientemente quimioterapia (8%) o radioterapia (8%). Los pacientes sometidos a colecistectomía tuvieron menor probabilidad (P < 0.05) de tener ictericia.
• TABLA 3: Comorbilidades pro procedimiento quirúrgico (Ver tabla)
Resultados
Los resultados por procedimiento quirúrgico se presentan en la Tabla 4. La tasa de mortalidad entre los 424 pacientes que recibieron un procedimiento potencialmente curativo fue del 4,6%. La mortalidad fue mayor (P < 0,01) en los pacientes sometidos a hepatectomía extendida (16%) o a un procedimiento paliativo (15%). Similarmente, la morbilidad grave fue mayor (P < 0,01) en los grupos de hepatectomía extendida (24%) y paliativo (28%). Ese patrón fue también verdadero para la morbilidad global. Los pacientes con hepatectomía extendida tuvieron una mayor probabilidad (P < 0,02) de volverse dependientes del respirador (12%), de desarrollar una ITU (8%), sepsis (12%) o shock séptico (12%). Los pacientes del grupo paliativo también tuvieron una mayor probabilidad (P < 0,02) de desarrollar una ISQ superficial (13%), insuficiencia renal (5%), ITU (12%) o sepsis (20%). Como resultado de ello, la mediana de la duración de la estadía fue mayor en la hepatectomía extendida (8 días) y en los pacientes con paliación (9 días; P < 0,001).
• TABLA 4: Resultados por procedimiento quirúrgico (Ver tabla)
Discusión
El ACS-NSQIP Participant Use File fue consultado para caracterizar los resultados, a corto plazo, de las operaciones en los pacientes con cáncer de vesícula en Norteamérica. Durante un período de 5 años, 613 pacientes fueron operados en 243 hospitales. Se realizó una operación potencialmente curativa en el 69% de los casos, mientras que las operaciones diagnósticas y paliativas fueron llevadas a cabo en el 13% y 6% de los pacientes, respectivamente. La hepatectomía parcial fue el procedimiento potencialmente curativo más frecuentemente realizado (59%), seguida por la colecistectomía (35%) y la hepatectomía extendida (6%). Los pacientes sometidos a hepatectomía extendida fueron significativamente más jóvenes y más sanos, mientras que aquellos sometidos a procedimientos paliativos fueron más ancianos y tuvieron mayor probabilidad de tener pérdida de peso y de haber recibido quimio o radioterapia. La morbilidad grave, la morbilidad global y la mortalidad, fueron peores para aquellos con hepatectomía extendida y procedimientos paliativos.
A pesar del pobre pronóstico del cáncer de vesícula en estadio avanzado, varios estudios recientes han mostrado que la resección agresiva puede mejorar la sobrevida a largo plazo [7,11,16-18]. En una revisión retrospectiva de datos de Surveillance, Epidemiology and End Results (SEER), Jensen y col. [18], mostraron que la resección radical es vastamente subutilizada en Norteamérica. Aunque algunas series han demostrado un aumento en la tasa de resecciones concomitantes del hígado con el paso del tiempo [7,11], los reportes de la experiencia norteamericana generalmente se han limitado a series de centros académicos aislados [5,7,11,19]. El presente análisis es consistente (6%) con los datos de SEER (10%) en que la tasa de hepatectomía extendida por cáncer de vesícula es baja, en relación con las tasas reportadas en Asia.
En comparación con los estudios norteamericanos mencionados, las series de Japón y China reportan una tasa más grande de resecciones extendidas, yendo dese el 30% al 60%, cuando se tratan cánceres de vesícula en estadio avanzado [10,14,17,20,21]. Esas tasas son difíciles de comparar con el presente estudio, porque su análisis incluye a pacientes sometidos a tratamiento para todos los estadios. Sin embargo, el manejo agresivo de la enfermedad avanzada, incluyendo la hepatectomía extendida, duodenopancreatectomía, disección ganglionar linfática extendida y resección vascular combinada, han sido apoyadas por algunos centros en Norteamérica [13,14]. De manera similar a este reporte, esas series japonesas y chinas documentan una tasa alta de morbilidad y mortalidad perioperatorias en pacientes sometidos a resecciones extensas. Se ha demostrado una buena sobrevida a largo plazo si se lograban márgenes negativos [10,14].
En este análisis del ACS-NSQIP, un porcentaje sustancial de los pacientes (24%) sometidos a una operación por cáncer de vesícula, recibieron sólo una colecistectomía. Ese hallazgo es importante, porque las guías actuales de la National Comprehensive Cancer Network recomiendan la resección radical de la fosa vesicular como el tratamiento óptimo para el cáncer de vesícula en estadio temprano [22]. Los pacientes sometidos sólo a colecistectomía tuvieron una mayor probabilidad de ser más añosos que los pacientes con hepatectomía parcial o extendida. La alta mortalidad observada en esos pacientes (7%), así como en aquellos sometidos a procedimientos diagnósticos (9%) puede ser explicada, en parte, por la extensa enfermedad metastásica al momento de la presentación.
Dada la naturaleza de la base de datos ACS-NSQIP, otros pacientes en ese grupo pudieron haber tenido un descubrimiento incidental de cáncer de vesícula y pudieron haber recibido subsecuentemente una operación más definitiva. Los reportes de Norteamérica sugieren que un tercio a la mitad de los pacientes derivados a centros terciarios por cáncer de vesícula, tuvieron una colecistectomía laparoscópica o a cielo abierto realizada antes de ser derivados [7,12]. Esos pacientes deberían ser considerados para una “colecistectomía extendida” después de una evaluación apropiada para excluidor toda evidencia de metástasis [23]. En contraste, si los pacientes tenían tumores T1a, la colecistectomía sola puede ser considerada un tratamiento definitivo [19].
En este reporte de los datos del ACS-NSQIP la hepatectomía parcial fue el procedimiento quirúrgico más frecuentemente realizado para el cáncer de vesícula. Esos procedimientos de “colecistectomía extendida” tuvieron tasas bajas de morbilidad y mortalidad y, por lo tanto, fueron seguros. Ese hallazgo es consistente con la tendencia general en el manejo del cáncer de vesícula en la última década [7,11,19,24]. El órgano con mayor probabilidad de ser invadido por el cáncer de vesícula es el hígado adyacente. Existe un debate considerable sobre el rol de otros procedimientos, tales como: (a) la extensión de la disección ganglionar linfática local, (b) si el conducto biliar debe ser rutinariamente resecado y (c) si está indicada la resección portal cuando se realiza una “colecistectomía extendida” [24]. Desafortunadamente, la base de datos ACS-NSQIP de 2005-2009 no brinda información sobre esos tópicos, lo que es una limitación importante de este reporte.
El examen cuidadoso del estado funcional preoperatorio, debería guiar la selección de pacientes para la resección hepática extendida, en pacientes con cáncer de vesícula avanzado [5,14]. La resección curativa puede lograr sobrevida a largo plazo en pacientes seleccionados, aun con enfermedad en estadio IV [10]. La morbilidad y mortalidad perioperatorias para esos procedimientos siguen siendo altas y es un factor potencialmente limitante para el uso expandido de esas operaciones [14,16,25]. El presente análisis confirma que, a pesar de una edad media más joven, clase ASA menor y mejor estado funcional de la cohorte sometida a resección extendida, las complicaciones postoperatorias, tales como la insuficiencia renal aguda, dependencia prolongada del respirador, shock séptico y muerte, fueron significativamente más grandes que en los otros grupos quirúrgicos. Esas observaciones sugieren que la realización de una operación aún más extendida, una hepático-duodenopancreatectomía combinada, se asociaría también con una morbilidad y mortalidad muy altas. Interesantemente, ninguna de esas operaciones fueron capturadas en la base de datos ACS-NSQIP durante el período de 5 años, lo que puede sugerir que los cirujanos norteamericanos consideran los resultados de esa operación muy radical como prohibitivamente altos.
El presente reporte debe considerarse a la luz de varias limitaciones adicionales. Primero, el ACS-NSQIP no recolecta información sobre radiología vesicular o hepática. El conocimiento sobre qué proporción de colecistectomías realizadas por cáncer de vesícula tuvo hallazgos radiográficos preoperatorios sospechosos de malignidad, podría ser de ayuda para interpretar esos datos. Segundo, una limitación mayor es la falta de datos anatomopatológicos. Como resultado, el estadio del tumor no pudo ser determinado y no se puede abrir juicio sobre si la colecistectomía, la hepatectomía parcial o la extendida, fueron aplicadas apropiadamente. Tercero, algunas complicaciones de interés particular cuando se realizan operaciones hepatobiliares (por ej., filtraciones biliares y falla hepática) no fueron consignadas en el período 2005-2009. El ACS-NSQIP ha reconocido esas limitaciones y está implementando numerosas variables específicas de la hepatectomía en 2013, tales como ictericia preoperatoria y drenaje biliar, embolización venosa portal, procedimientos concomitantes como resección de conductos biliares, filtraciones biliares, falla hepática, así como estadios T, N y M.
Cuarto, sólo la mortalidad dentro de los 30 días es suministrada por el ACS-NSQIP. Para la hepatectomía, es preferible la mortalidad dentro de los 90 días. Quinto, la información de la sobrevida a largo plazo no está disponible en el ACS-NSQIP. Esa limitación es importante también, porque la influencia de los resultados a corto plazo sobre la sobrevida global o la libre de enfermedad no pueden ser determinadas, aunque podría esperarse que fuera relevante. Finalmente, los hospitales participantes en el ACS-NSQIP tienen una mayor probabilidad de ser grandes centros académicos que, generalmente, tienen énfasis en la mejora de la calidad. Aunque ese factor puede limitar la generalización, ha ocurrido una significativa regionalización de la hepatectomía, en centros con alto volumen de pacientes, en la década pasada.
En conclusión, este análisis de una cohorte multicéntrica grande en Norteamérica, sugiere que la hepatectomía parcial es el procedimiento realizado más comúnmente y con mayor seguridad para el cáncer de vesícula. La cirugía paliativa no es efectuada comúnmente, quizás a causa de la alta morbilidad y mortalidad asociadas. Una minoría pequeña de pacientes más jóvenes y más sanos, es sometida a hepatectomía extendida, pero la morbilidad y mortalidad de esa operación es mucho mayor, comparada con procedimientos menores. En consecuencia, toda ventaja potencial a largo plazo de la cirugía extendida, para el cáncer de vesícula, debe ser atemperada por el riesgo aumentado a corto plazo. Asimismo, la baja tasa de hepatectomía extendida en esta cohorte sugiere que los cirujanos en Norteamérica pueden ser menos agresivos que algunos pares internacionales, persiguiendo una resección muy radical para el cáncer de vesícula. Ese abordaje puede ser apropiado, a la luz del riesgo aumentado, en el corto plazo, de la cirugía extendida. El presente análisis sugiere también que los pacientes con cáncer de vesícula deberían ser manejados en centros con alto volumen de casos, con experiencia con esos enfermos complejos.
♦ Comentario y resumen objetivo: Dr. Rodolfo D. Altrudi
.jpg)